認知症各論(2)
(4)アルツハイマー型認知症のバイオマーカー診断
バイオマーカーを標的にした PET(Positron Emission Tomography)
- 陽電子(ポジトロン)を放出する放射性同位元素で標識された薬剤を被験者に投与し、その分 布を PET カメラで断層画像に撮影することにより、臓器(脳)の局所機能を画像に描き出す検査 法である。
アミロイドβ蛋白(アミロイド PET:トレーサー:11C-PiB)や、Tau 蛋白(Tau-PET)の 脳内蓄積状態(どの場所に、どの程度)を可視化することにより、アルツハイマー型認知症の早期 診断や将来発症のリスク予測、その他の認知症の病態研究のために有用な手段となっている。
また、認知症の原因となり得るこれらの物質に対する治療薬の開発に関連し、その薬剤の有効性 を評価する上でも重要な武器となっている。
但し、現時点では、診断薬、画像診断装置は極めて高額であり、保険適応となっていないため実 臨床での使用には限界がある(検査には、10万〜20万円かかる)。
(これらの詳細は成書に譲る)
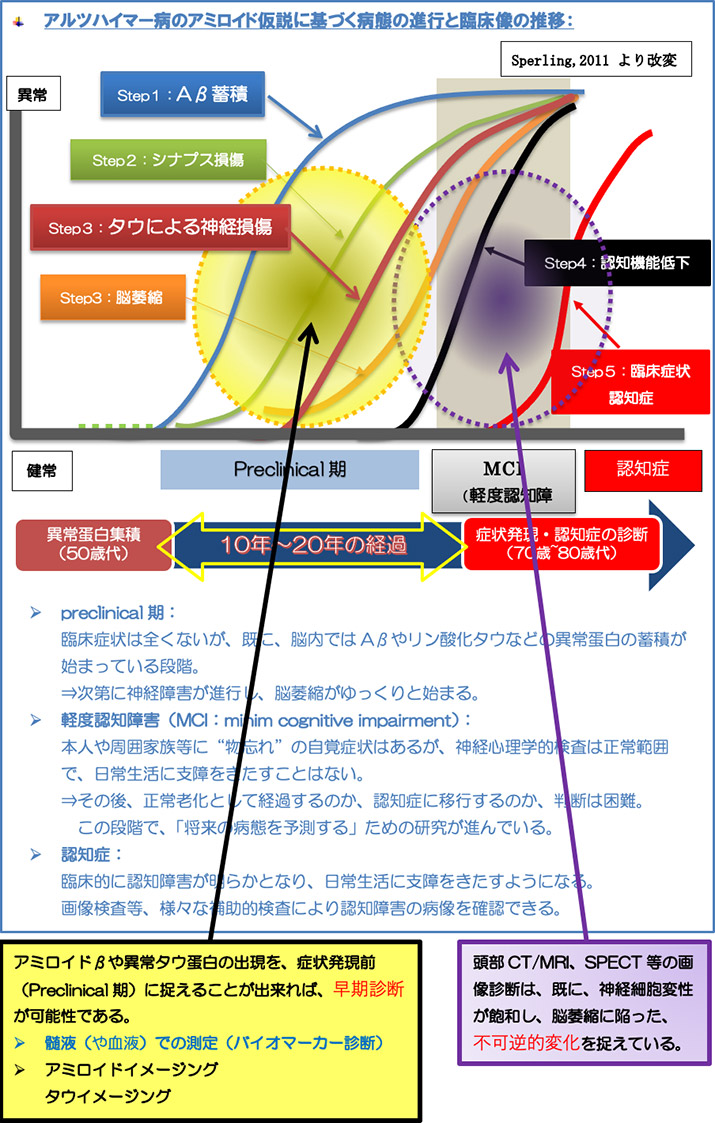
アミロイドイメージングの臨床への応用
- アミロイド PET により、早い段階(症状発現前の若年期)でアミロイドβの沈着を確認で きれば、将来のアルツハイマー病の発症を予測できる。
ATN 分類(Jack、Alzheimers Dement,:2018より改変)
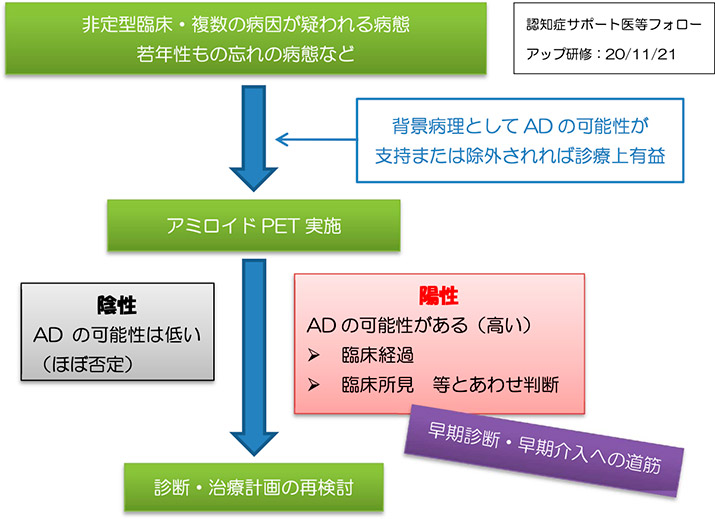
- 上述の実用化されたいくつかの診断技術の結果を組み合わせて認知症の診断をする試み
(認知症サポート医等フォローアップ研修:岩田 淳より抜粋)
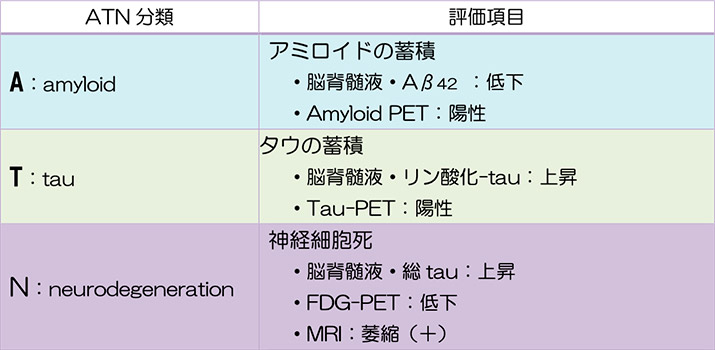
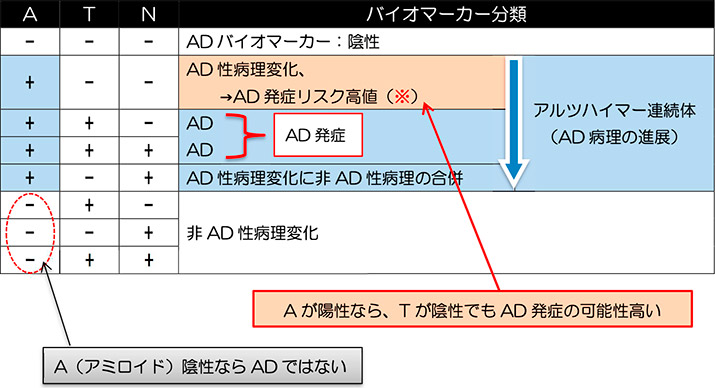
ATN 分類による診断
最近の知見:血中バイオマーカー(アミロイドβ)測定

(5)アルツハイマー型認知症の治療:薬物療法
前述したように、アルツハイマー型認知症の病態に関しては多くの解決されなければならない 問題があり、それ故、現時点で決定的かつ有効な治療法は見つかっていない。
「認知機能を元に戻す」、あるいは「少なくとも症状を進行させない」ことを可能とする治療薬はなく、「症状の進行を遅らせる」ことしかできないのが現状である。
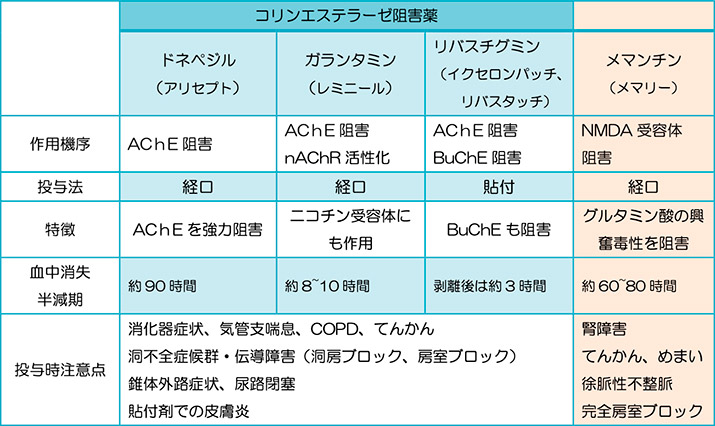
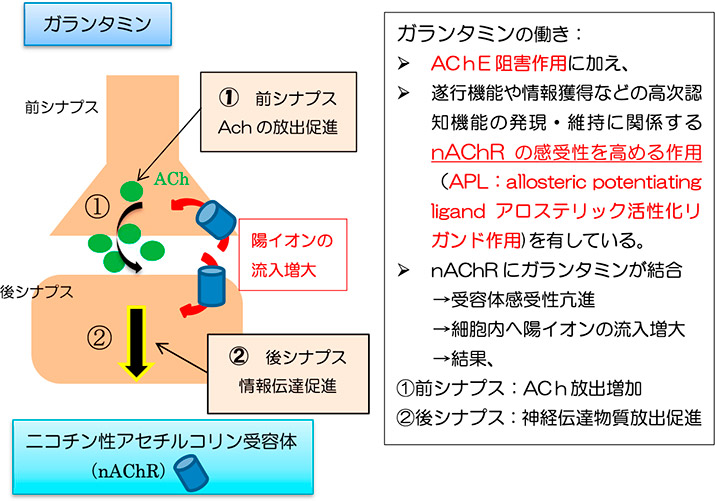
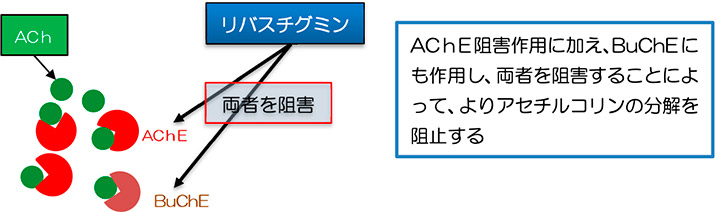
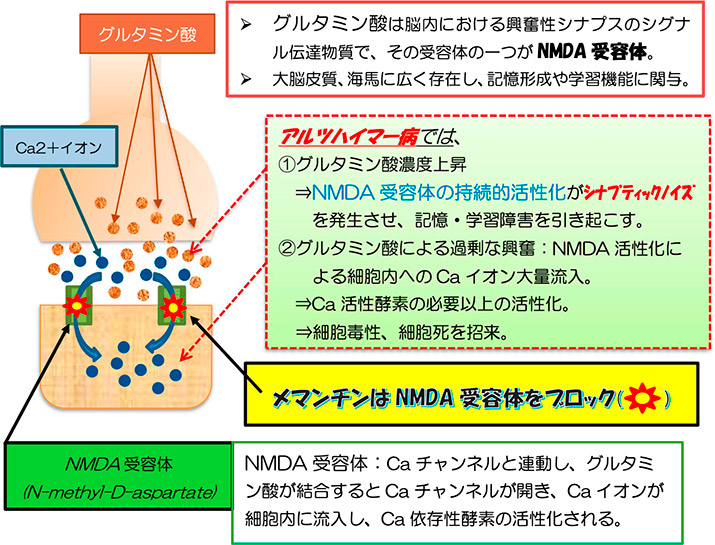
コリンエステラーゼ阻害薬(基本的な薬剤)

現在認められている抗認知症薬
抗認知症薬の大まかな使い方
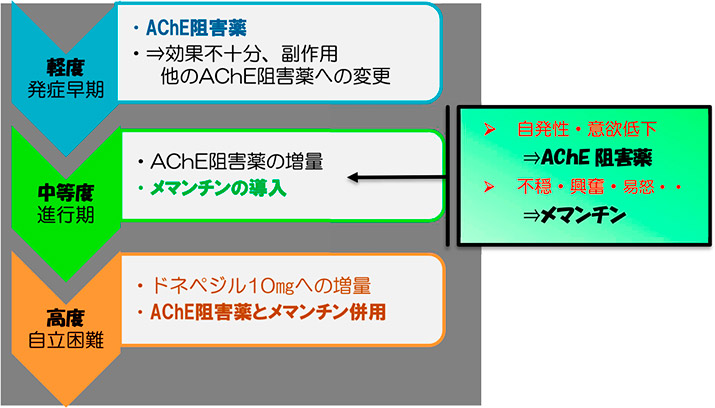

現在認可されているこれらの認知症薬(コリンエステラーゼ阻害薬等)は、「アルツハイマー 型認知症」と診断された段階で使用され、部分的な効果が認められてはいるものの、ADを治癒させることや、その後の病状の進行を抑えこむことはできない。なぜなら、既に認知症を発症した状態で認められる病態のある部分を標的にした治療にしか過ぎず、認知症の根本的な病因に対する治 療ではないからである。
これらの薬剤の役割は「病気の進行を遅らせる」ことにとどまっているのが現状である。
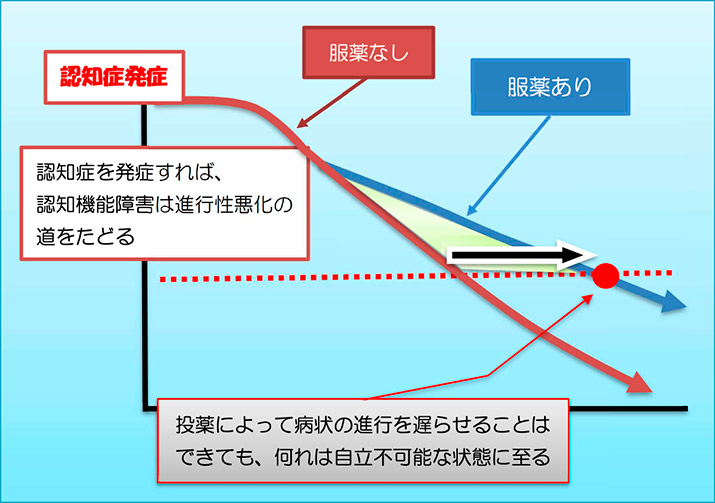
これ等薬剤が投与される段階は、病状が進行し、既に不可逆的な脳萎縮(脳細胞の死滅状態)が それなりに完成した局面であり、アルツハイマー病の本質的な病因の一つと考えられている「アミロイドβ蛋白の沈着」は、我々が病気として認識できる「認知症」が明らかとなるおよそ20年近くも前から始まっていることが明らかとなっている。
「Aβ蛋白の沈着」は留まることなく粛々と進行し、認知機能障害は確実に進行する。
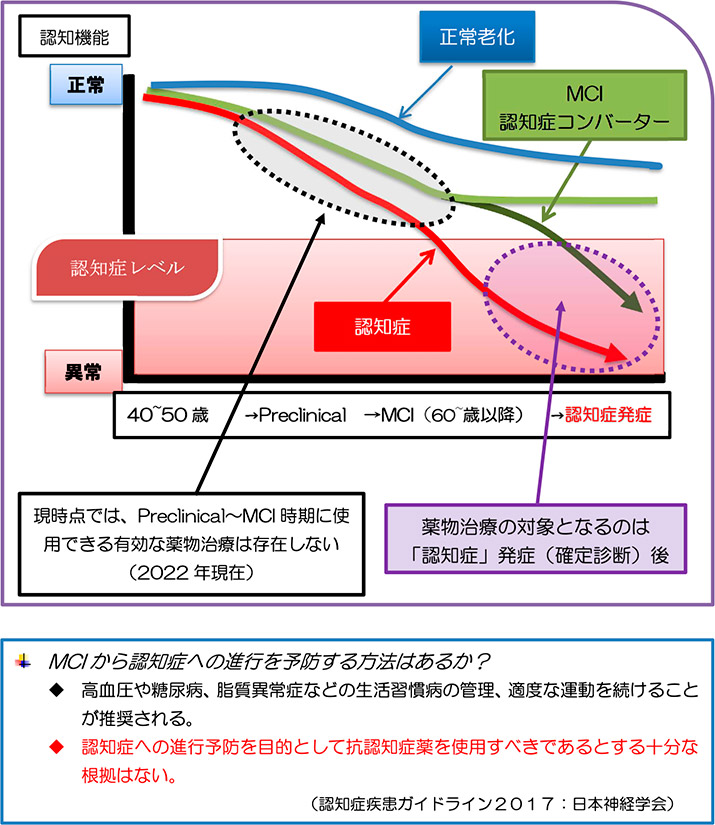
「認知症」として認識されるおよそ20年前の40〜50歳台から、既に、病気の芽が存在していることを考慮すると、根本的治療のためにはこの時点での早期発見、早期介入が必須である。
最近、Aβ蛋白の除去作用を有する抗アミロイドβ抗体薬が米国FDAにより認可されたが、すでに認知症を発症してしまった症例に対する臨床効果の評価は道半ばである。
その概要を下記に示した。
抗認知症薬:aducanumab に関する指針
米国神経学会 ポジション・ステートメント(倫理的指針)
Neurology 2021.11.17 オンライン版から

同薬は脳内の異常蛋白質 Aβを減少させる一方で、Aβの減少が患者に臨床的ベネフィッ ト(認知機能の改善)をもたらすかは未だに不明と結論。その上で、同薬投与例では MRI で 観察されるアミロイド関連画像異常:ARIA(Amyloid related imaging abnormalities: Sperling, 2011)のリスクがあり、3割で脳浮腫、2割で脳微小出血が認められたことか ら、頻回な MRI によるモニタリングが必要であるとしている。
※ARIA は血管に付着した Aβに対する攻撃の結果と考えられている。
行うべき情報提供(インフォームドコンセント)
- ① 中等度または進行した AD患者、脳内にAβの蓄積が見られない患者に aducanumabで治療を行うべき十分な根拠はない。
- ② aducanumabはADを治癒に導いたり、認知機能を回復させない。
- ③ 潜在的な副作用に留意し、MRI によるモニタリングを頻回(治療前と後)に行う必要がある
- ④ 年間約5万6千ドル(約 640万円)の薬剤費を要し、経済的負担を伴う。
- ⑤ 臨床試験においては、人種的、民族的多様性データが不足しており、過小評価されている集団や患者に対する有効性や安全性のデータが欠如している。

有効な治療薬が存在しない現在、なすべきことは?
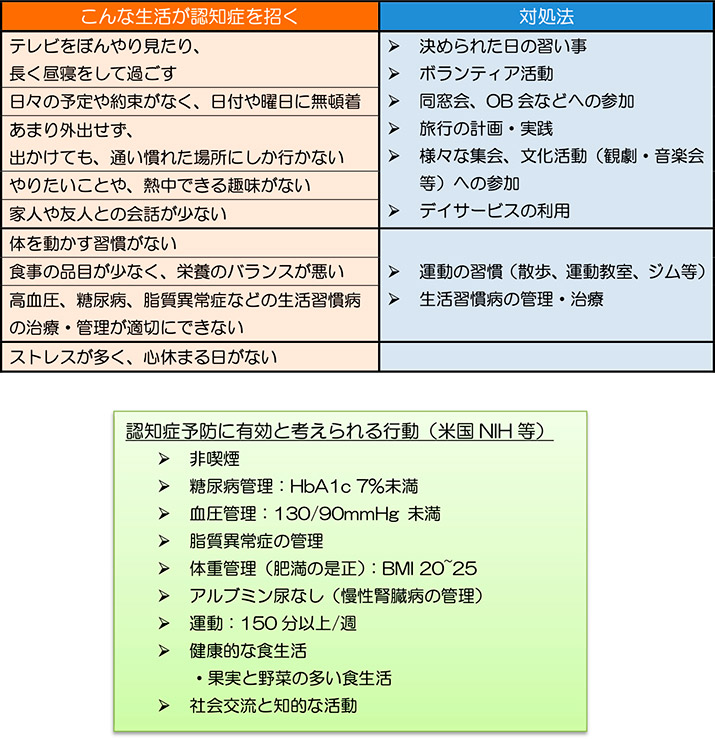
- 有効な治療薬が存在しない一方で、様々な疫学的研究等から生活習慣改善が認知症の予防に有効であることが分かっている。
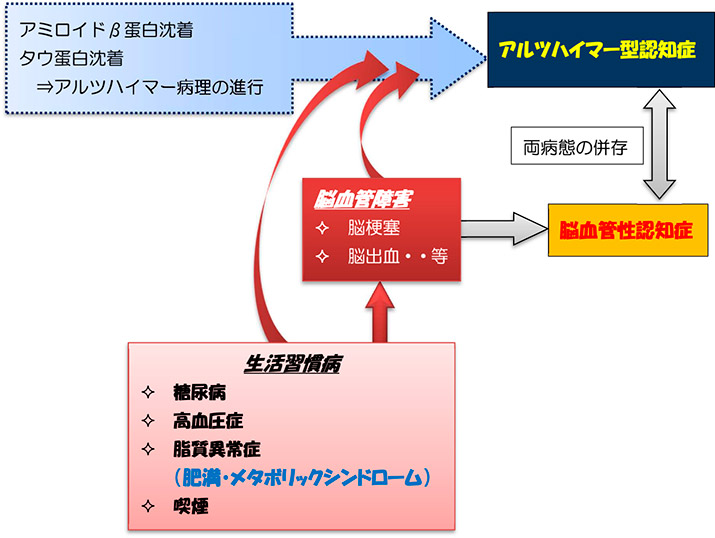
- ・肥満やメタボリックシンドロームなどを基盤として起こる糖尿病、高血圧症、脂質異常症は、それぞれが Aβ蛋白代謝に負の影響を与え、認知障害の進行に深くかかわっていることが分かってきている。
- ・また、これら生活習慣病は脳血管障害(脳梗塞、脳出血)の強力な危険因子であり、 脳血管障害を発症することで脳血管性認知症の原因となる。
- ・同一患者においてアルツハイマー型認知症と脳血管性認知症が併存・合併する例はしばしば認められ、これらケースでは認知障害の程度はより大きくなる。
- ・認知症発症予防、認知症病態の進行抑制のためには、これら生活習慣病の厳格管理が 極めて重要である。
今行うべき「認知症予防行動」